傾儖僐乕儖偺斀墳惈偼戞堦媺丒戞擇媺丒戞嶰媺偱堎側傝傑偡偑丄偦偺偳傟偵傕嫟捠偡傞斀墳傪彂偄偰偄偒傑偡丅
侾丏傾儖僇儕嬥懏偲偺斀墳
俀丏僴儘僎儞壔悈慺偲偺斀墳
俁丏扙悈斀墳
斀墳偼嫟捠偟偰婲偒傑偡偑丄斀墳偺偟傗偡偝偼曄傢偭偰偒傑偡丅
侾丏傾儖僇儕嬥懏偲偺斀墳
傾儖僐乕儖偵僫僩儕僂儉側偳偺梲惈偺嫮偄嬥懏傪壛偊傞偲丄僸僪儘僉僔儖婎俷俫偺俫偑俶倎偵抲姺偝傟丄俫俀偑敪惗偟偰僫僩儕僂儉傾儖僐僉僔僪偑惗惉偝傟傑偡丅
俀俠2俫5俷俫亄俀俶倎仺丂丂丂俀俠2俫5俷俶倎丂丂丂亄俫2仾
丂丂丂丂丂丂丂丂丂僫僩儕僂儉傾儖僐僉僔僪
亙僫僩儕僂儉傾儖僐僉僔僪亜堦斒幃俼-俷俶倎
傾儖僐乕儖偺僸僪儘僉僔儖婎偺俫偑丄俶倎偵側偭偨壔崌暔傪巜偟傑偡丅
柦柤朄偼丄傾儖僉儖婎俼偺岅旜乽傿儖乿傪乽僅僉僔僪乿偵姺偊偰丄偦偺慜偵僫僩儕僂儉傪偮偗傑偡丅
塸岅昞婰偩偲乽yl乿傪乽oxid乿偵姺偊偰偄傞偙偲偵側傝傑偡丅
椺丏
僄僞僲乕儖佀僫僩儕僂儉僄僩僉僔僪丂丂丂僾儘僷僲乕儖佀僫僩儕僂儉僾儘億僉僔僪
ethanol佀sodiumethoxid丂丂丂丂丂丂丂丂丂丂丂propanol佀sodiumpropoxid
俠2俫5俷俫佀俠俫3俠俫2俷俶倎丂丂丂丂丂丂俠3俫7俷俫佀俠3俫7俷俶倎
僫僩儕僂儉傾儖僐僉僔僪偼丄悈偵梟偗傞偲壛悈暘夝偟偰嫮墫婎惈傪帵偟傑偡丅
俠2俫5俷俶倎亄俫2俷仺俠2俫5俷俫亄俶倎俷俫
傑偨僫僩儕僂儉偺戙傢傝偵僇儕僂儉傪梡偄偰傕摨條偵斀墳偟丄僇儕僂儉傾儖僐僉僔僪偑惗惉偝傟傑偡丅俀丏僴儘僎儞壔悈慺偲偺斀墳
傾儖僐乕儖偵擹墫巁側偳偺擹僴儘僎儞壔悈慺巁傪壛偊傞偲丄僸僪儘僉僔儖婎偑僴儘僎儞偱抲姺偝傟傑偡丅
俠2俫5俷俫亄俫俠倢仺丂丂俠2俫5俠倢丂丂亄俫2俷
丂丂丂丂丂丂丂丂侾亅僋儘儘僄僞儞
椺偵嫇偘偨斀墳偼乮昅幰偼傑偩帋偟偰偄側偄偺偱曐徹偼弌棃傑偣傫偑乯偨傇傫丄偐側傝婲偙傝偵偔偄偲巚傢傟傑偡(徫)扨偵彂偒傗偡偔偰嫵偊傗偡偄偐傜嫵壢彂偵嵹偭偰傞傫偱偟傚偆偹丅
偙偺斀墳惈偺嵎傪梡偄偰丄傾儖僐乕儖偑戞壗媺側偺偐傪挷傋傞偙偲偑弌棃傑偡丅
擹棸巁偵怗攠偲偟偰倅値俠倢俀傪梟偐偟偨帋栻傪儖乕僇僗帋栻偲偄偄傑偡丅傾儖僐乕儖偵儖乕僇僗帋栻傪壛偊傞偲丄
戞堦媺傾儖僐乕儖丗忢壏偱偼斀墳偣偢壛擬偑昁梫側偨傔丄斀墳偟側偄丅
戞擇媺傾儖僐乕儖丗斀墳奐巒傑偱偵悢暘傎偳偺帪娫傪梫偡傞丅
戞嶰媺傾儖僐乕儖丗悢昩偱敀怓捑揳傪惗偠傞丅
偲偄偆堘偄偑惗偠傑偡丅偙偺斀墳偺條巕偐傜傾儖僐乕儖偺幆暿偑壜擻偱偡丅
偙傟傪儖乕僇僗帋尡偲偄偄傑偡丅
俁丏扙悈斀墳
傾儖僐乕儖偺扙悈斀墳偼丄暘巕撪扙悈偲暘巕娫扙悈偺俀庬椶偑婲偙傝傑偡丅
暘巕撪扙悈丗侾暘巕撪偱悈侾暘巕偑扗傢傟傞斀墳
暘巕娫扙悈丗俀暘巕娫偱悈侾暘巕偑扗傢傟傞斀墳
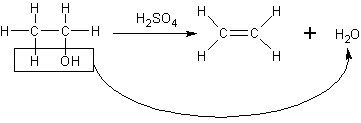
僄僞僲乕儖偵擹棸巁傪壛偊丄侾俇侽乣侾俈侽亷偵壛擬偡傞偲丄僄僠儗儞偑惗惉偟傑偡丅
俠俀俫俆俷俫仺俠俫俀=俠俫俀亄俫俀俷丂乮怗攠丗俫俀俽俷係乯
偙傟偼丄僄僠儗儞偺幚尡幒揑惢朄偺偲偙傠偱堦搙尒傑偟偨偹丅偙偺斀墳傪徻偟偔尒偰傒傞偲丄師偺傛偆偵僸僪儘僉僔儖婎偲椬偺俫偑扗傢傟偰偄傞偺偑暘偐傝傑偡丅
俛丏暘巕娫扙悈
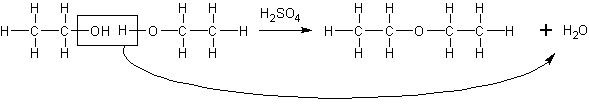
僄僞僲乕儖偵擹棸巁傪壛偊丄侾俁侽乣侾係侽亷偵壛擬偡傞偲丄僕僄僠儖僄乕僥儖乮屻弎乯偑惗惉偟傑偡丅
俀俠俀俫俆俷俫仺俠俀俫俆-俷-俠俀俫俆亄俫俀俷丂乮怗攠丗俫俀俽俷係乯
偙偺斀墳偺傛偆偵丄俀偮偺暘巕偐傜娙扨側暘巕偑扗傢傟偰俀暘巕偑寢崌偡傞斀墳傪弅崌偲偄偄傑偡丅崱搙偼丄曅曽偺僄僞僲乕儖偺帩偮僸僪儘僉僔儖婎偲傕偆曅曽偺帩偮俫偑扗傢傟偰偄傞偙偲偑暘偐傝傑偡丅
傾儖僐乕儖偺扙悈斀墳偱偼丄戞嶰媺傾儖僐乕儖偑堦斣扙悈偝傟傗偡偔丄戞擇媺丄戞堦媺偺弴偵扙悈偝傟偵偔偔側傝傑偡丅
傑偨丄暘巕撪扙悈偟偰傾儖僉儞偑敪惗偡傞偐丄暘巕娫扙悈偟偰僄乕僥儖偑惗惉偡傞偐偼丄斀墳壏搙偵傛偭偰寛傑傝傑偡丅偙偙偱偺斀墳偺傛偆偵丄斾妑揑崅壏搙偩偲傾儖僉儞丄斾妑揑掅壏搙偩偲僄乕僥儖偑惗惉偟傑偡丅
